Naučnici su otkrili novi način za suzbijanje mutacija koje dovode do širokog spektra genetskih poremećaja.
Studija nedavno objavljena u časopisu Molecular Cell opisuje strategiju koja kooptira normalan proces modifikacije RNK unutar ćelija kako bi se geni bolesti transformisali u normalne gene koji proizvode zdrave proteine. Nalazi su značajni jer na kraju mogu pomoći istraživačima da promene tok razornih poremećaja kao što su cistična fibroza, mišićna distrofija i mnogi oblici raka.
Oko 15% mutacija koje dovode do genetskih bolesti nazivaju se besmislene mutacije. Prikladno nazvane, besmislene mutacije nastaju kada molekul iRNK sadrži rani signal „zaustavljanja“. Kada mRNA uzme genetske instrukcije od DNK za stvaranje proteina, ovaj znak ranog zaustavljanja naređuje ćeliji da prestane da čita uputstva tokom procesa. To dovodi do stvaranja nekompletnog proteina koji može dovesti do bolesti.
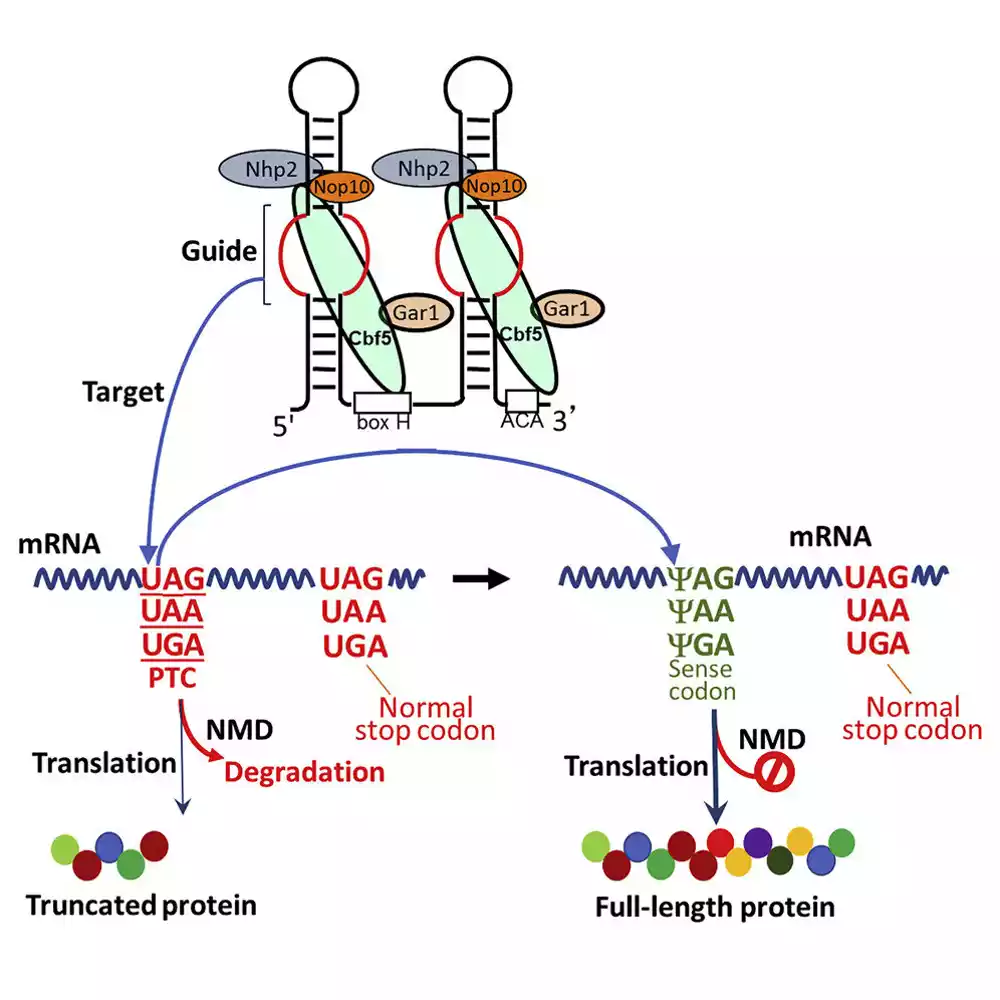
Predvođeni dr Ji-Tao Juom, tim istraživača iz Centra za biologiju RNK Univerziteta u Ročesteru dizajnirao je veštačku RNK-vodiču — deo RNK koji može da modifikuje druge tipove RNK — da cilja molekule mRNA koji sadrže ranu signali zaustavljanja (koji se takođe nazivaju kodoni prevremenog završetka). Vodiće RNK su prirodni mehanizam koji ćelije koriste sve vreme; Iu-ov tim je promenio ovaj već postojeći proces.
Kao i DNK, RNK se sastoji od molekularnih građevinskih blokova koji su predstavljeni slovima A (adenin), G (gvanin), U (uracil) i C (citozin). Kodoni prevremenog prekidanja uvek imaju gradivni blok U na prvoj poziciji (na primer, UAG, UAA ili UGA). Veštačka RNK vodiča tima je dizajnirana da modifikuje U na prvoj poziciji, menjajući molekularni sastav ciljane mRNK tako da ćelija više ili manje dobro prepozna stop signal.
Tim, uključujući Paul Boutza, Ph.D., docenta za biohemiju i biofiziku; postdiplomci Ji Pan i Sjuejang He; postdoktorski saradnik Džonatan Čen; naučnik Hironori Adachi; a istraživači iz ProKR Therapeutics testirali su veštačku vodeći RNK u ćelijama kvasca i u ćelijama bolesti kod ljudi (proisteklih iz pacijenata sa cističnom fibrozom i neurofibromatozom). U oba slučaja, otkrili su da je dejstvo veštačke RNK vodiča učinilo prevremeni terminacioni kodon (znak stop) nevidljivim, omogućavajući ćelijama da pročitaju genetska uputstva do kraja i stvore funkcionalne proteine pune dužine.
Takođe su otkrili da je vodeća RNK potisnula drugi mehanizam u ćeliji poznat kao raspad mRNA posredovan besmislom ili NMD. Jedan od glavnih sistema nadzora u telu, NMD cilja i eliminiše mRNK sa kodonima prevremenog završetka, tako da se protein ne proizvodi. Obuzdavanje NMD-a je još jedan način na koji je veštačka vodeći RNK osigurala da je značajna količina mRNK prisutna u ćeliji, i da su genetske instrukcije koje nose ciljane mRNK pročitane do kraja i prevedene u kompletne proteine.
Cistična fibroza (CF) je jedno od mnogih stanja koje mogu biti rezultat besmislene mutacije. Kod CF, besmislena mutacija u CFTR genu dovodi do proizvodnje nekompletnih CFTR proteina, koji su odgovorni za regulisanje protoka soli i tečnosti u i iz ćelija. Rezultat je nakupljanje guste sluzi i uporne infekcije pluća koje karakterišu stanje. Iu veruje da strategija njegovog tima za suzbijanje besmislenih mutacija u genima bolesti ima veliki potencijal da pomogne pacijentima sa CF i mnogim drugim naslednim genetskim bolestima.
„Naša tehnika je obećavajuća jer nismo primetili nikakve negativne efekte van cilja. Koristeći jednu vodeću RNK u bolesnim ćelijama – i ništa drugo – možemo posebno da potisnemo besmislene mutacije bez ometanja drugih delova ćelije“, primetio je Ju, dekanski profesor biohemije i biofizike na Medicinskom i stomatološkom fakultetu Univerziteta u Ročesteru. „Uvek postoji zabrinutost oko specifičnosti kod genskih terapija na nivou DNK, jer su promene u DNK trajne. Pošto je RNK prolazna, manje je brige o dugotrajnim efektima. RNK vođena modifikacija RNK nam daje ogromnu moć da ciljamo na nulu. jednu tačku u genomu i napraviti veoma precizne promene.“
„Istraživanje dr Ju je na čelu najperspektivnijih modaliteta lečenja cistične fibroze i potencijalno drugih genetskih bolesti“, rekao je dr Džefri Džej Hejz, predsedavajući i Šohei Koide profesor biohemije i biofizike na Univerzitetu u Ročesteru Medicinski i Stomatološki fakultet. „Ovo su zaista uzbudljiva vremena.“